Questions fréquemment posées sur l’introduction du test HPV dans le dépistage du cancer du col de l’utérus en Belgique
Pour des questions spécifiques concernant la NOMENCLATURE (codes, remboursement, notification, etc.) : Dépistage primaire du cancer du col de l’utérus par HPV | INAMI
Pour les questions techniques concernant le test HPV : voir les «Questions fréquentes» : Centre National de Référence (CNR) pour le Papillomavirus humain | sciensano.be
Pour les questions spécifique concernant l’INSCRIPTION : Bulletins d’information | Belgian Cancer Registry / En général | Belgian Cancer Registry
Général
- Q: Que devons-nous faire par rapport aux recommandations faites en 2024 des suivis diagnostiques (nouveau test après 6 mois au lieu de la nouvelle recommandation après 1 an) ?
-
R: Les bénéficières dont le dépistage était positif en 2024 et qui ont reçu l’ancienne recommandation peuvent continuer à assurer le suivi proposé. Elles bénéficieront d’un frottis de suivi remboursé après 6 mois au lieu des 12 mois désormais prévus dans le nouvel algorithme (en 2025), mais un seul remboursement par année civile. Après ce suivi diagnostique remboursé (à 6 mois), des conseils seront donnés conformément au nouveau calendrier de dépistage. En d’autres termes, le patient sera orienté vers un dépistage de routine ou une colposcopie — en fonction des résultats du ou des test(s). Le nouveau test de suivi doit également être conforme aux nouveaux algorithmes de dépistage : cytologie pour les 25-29 ans, test HPV pour les 30-64 ans.
- Q: Si un patient obtient un résultat de dépistage anormal mais revient au programme de dépistage normal au bout de suivi de 12 mois (2ème triage), le prochain dépistage a-t-il lieu 3 ou 4 ans après le dépistage initial ?
-
R: Le prochain dépistage pour les bénéficières après un premier résultat de dépistage anormal, mais avec un résultat négatif au 2ème triage (suivi après 12 mois), est effectivement 3 ans (pour la cytologie) ou 5 ans (pour un test HPV) après le dernier résultat de dépistage négatif. Cela signifie donc en réalité 4 ou 6 ans après le résultat du dépistage initial.
- Q: Dans le cas d’un patient dont le test HPV primaire est positif et qui — conformément à la directive scientifique de Sciensano — doit subir un test de suivi après 12 mois (2ème triage), comment faut-il choisir le moment de ce test de suivi pour que le patient soit assuré d’être remboursé. S’agit-il (au plus tôt) d’une année civile, ou existe-t-il éventuellement un intervalle de temps bien défini ?
-
R: « Après 12 mois » signifie littéralement au plus tôt après un intervalle d’un an. Il est préférable de ne pas le faire avant, étant donné le temps nécessaire pour éliminer une infection à HPV et permettre une éventuelle régression de la lésion, mais nous comprenons également que la programmation des examens de suivi ne peut pas se faire au jour le jour 12 mois plus tard. Il a été décidé de ne pas définir d’intervalles bien définis, mais de s’en remettre aux bonnes pratiques. Il n’est donc certainement pas question de remboursement pour le patient si cela se produit juste dans les 12 mois (avec une préférence pour une période légèrement plus longue que 12 mois compte tenu de ce qui précède) ou peut-être même avec un retard de quelques semaines/mois.
- Q: Comment doit-on assurer le suivi après une hystérectomie pour des lésions néoplasiques du col de l’utérus (carcinome épidermoïde ou adénocarcinome) ?
-
R: Le suivi des patientes atteintes d’un cancer du col de l’utérus (adéno et squameux) est très diversifié. Les stratégies de suivi varient d’un hôpital à l’autre; les directives internationales diffèrent également. La cytologie n’est pas la norme en matière de suivi, mais elle est utilisée dans certains hôpitaux. Il en va de même pour les scanners (TEP) et les marqueurs tumoraux. C’est pourquoi aucune directive belge n’a encore été élaborée.
Il est toujours possible d’effectuer un suivi sous l’indication « suivi (thérapeutique) ».
- Q: Chez les 65+ : après le suivi à 12 mois (2ème triage), pendant combien d’année le suivi annuel est-il remboursé?
-
R: Le suivi est indépendant de l’âge. Il n’y a qu’un seul suivi (à 12 mois, le 2ème triage)) qui donne une recommandation clinique finale aux personnes dépistées de plus de 65 ans, ainsi que le groupe cible plus jeune, et aucun autre suivi (annuel) ne devrait être nécessaire (sauf pour le suivi d’une infection prouvée par le hrHPV (postcolposcopie), le suivi après le traitement d’une CIN 2+, et aussi longtemps que le suivi est nécessaire selon la directive scientifique).

-
Q: Il y a une discordance entre la nomenclature et la directive scientifique de Sciensano concernant les tests à effectuer dans le cadre du dépistage des groupes à haut risque. La nomenclature définit le hrHPV ET la cytologie (553674-553685 pour le hrHPV et 591835-591846 pour la cytologie). En revanche, la directive scientifique de Sciensano fait la distinction entre :
DES/AIS : cotesting patients immunodéprimés : hrHPV OU cytologie selon l’âge (ce n’est pas inclus dans la nomenclature, mais selon la nomenclature, il s’agit également d’un cotesting). -
Le cotesting dans DES/AIS est toujours correct.
Pour les patientes immunodéprimées :selon la nomenclature — s’agissant d’un groupe à haut risque — un co-test (test HPV et cytologie simultanés) serait remboursé, mais « la directive scientifique » prescrit une cytologie OU un test HPV. Toutefois, des experts ont estimé qu’un co-test n’est pas nécessaire chez les patients immunodéprimés. Dans la « Directive Scientifique », vous trouverez les algorithmes de dépistage pour les jeunes femmes (21-29 ans) et les personnes âgées (30+) immunodéprimées. On peut y voir qu’une cytologie annuelle est recommandée pour les jeunes et un test HPV tous les trois ans pour les 30 ans et plus. Le co-test n’a donc pas été considéré comme le test le plus optimal dans ces indications.
L’état ‘Directive Scientifique’ :
Un seul et même code de nomenclature est fourni pour les tests réalisés dans le groupe de patientes à haut risque et les tests réalisés en cas d’indications cliniques (591835-591846 pour les examens cytologiques et 553674-553685 pour les tests HPV), sans restriction d’âge. Cependant, une fréquence de tests convenue par les experts est toutefois recommandée (voir 3.3-3.4). Il est de la responsabilité du médecin traitant de se conformer à la fréquence de tests de dépistage recommandée et au type de test recommandé (cotesting en cas de DES/AIS et test HPV ou examen cytologique pour les groupes de patientes immunodéprimées, en fonction de l’âge).
- Q : Les patients qui entrent dans la catégorie à haut risque (par exemple, DES ou immunosuppression), le dépistage s’arrête-t-il également chez eux à 65 ans ou se poursuit-il à vie (ou aussi longtemps que dure le traitement immunosuppresseur) ?
-
R : Pour les groupes à haut risque, il n’y a pas de limite d’âge pour les options de dépistage. Le dépistage peut être effectué dès que et aussi longtemps que cela s’avère nécessaire d’un point de vue médical.
-
Q : Après deux tests HPV négatifs, les patients ayant subi une conisation doivent continuer à se faire dépister tous les 3 ans pendant 25 ans, puis tous les 5 ans.
a) Comment ce test HPV triennal doit-il être facturé ? b) Si un résultat HPV positif est obtenu ici, la cytologie réflexe doit-elle être effectuée automatiquement au laboratoire ? -
A: a) La facturation via 149634-149645 pour la réalisation d’un frottis de suivi, pour le test HPV est de 553652-553663.
b) La cytologie réflexe devrait être effectuée automatiquement dans le cadre du suivi (post-colposcopique) en cas de résultat HPV positif.
- Q : En cas de cytologie antérieure anormale avec une PCR HPV négative (par exemple LSIL — HPV négatif en 2023), seule une PCR est demandée en 2025 et elle est négative. Le laboratoire doit-il alors ajouter une cytologie (réflexe) ?
-
R : Non, aucun test réflexe ne suit le résultat d’un test primaire négatif. De plus, un test HPV ne doit pas être réalisé dans les cas de LSIL (dans le nouvel algorithme de dépistage), car il n’apporte aucune information pertinente pour le suivi ou le traitement de la femme. Une cytologie de suivi (2ème triage) doit être demandée après 12 mois. Le critère d’évaluation étant la réorientation vers le dépistage systématique (en cas de NILM ou d’ASC-US/HPV négatif) ou la colposcopie (en cas d’ASC-US/HPV positif ou de >=LSIL).
Cependant, dans l’exception pour les résultats obtenus avant 2025 mentionnée au chapitre 4 du Directive Scientifique :4.2 Test HPV négatif avec cytologie ASC-US/LSIL (résultats de dépistage obtenus avant 2025)
- Test HPV-HR négatif avec LSIL
Les femmes présentant un résultat LSIL au test de dépistage ne doivent pas être orientées pour subir un test HPV, mais dans les rares cas où un cotest a été réalisé lors du précédent programme de dépistage, ces femmes devront refaire l’objet d’un test HPV dans les 12 mois. - Si le nouveau test montre un résultat négatif au test HPV-HR, la patiente peut être orientée en toute confiance vers un dépistage de routine.
- Si le résultat au nouveau test HPV est HPV-HR positif, la patiente devra être orientée vers une colposcopie immédiate, étant donné que le risque de CIN3+ à 5 ans est de 2,0 % (27).
- Test HPV-HR négatif avec LSIL
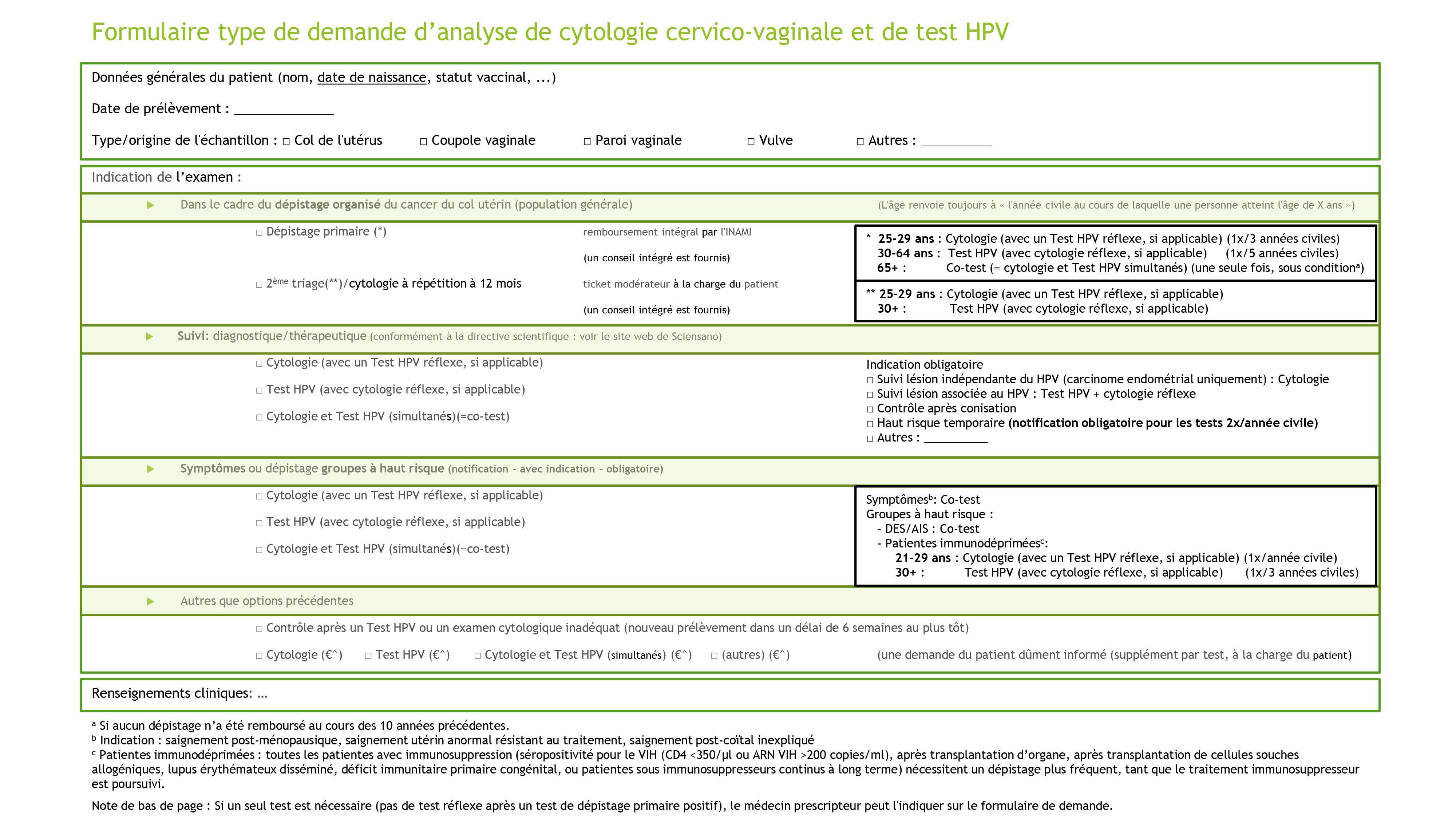
- Q : Existe-t-il un modèle de formulaire de demande pour la cytologie cervicovaginale et le test HPV dans le cadre du nouveau programme de dépistage du cancer du col de l’utérus ?
-
R : Oui, un modèle a été élaboré à titre de suggestion pour couvrir toutes les options du nouveau programme de dépistage. Il peut être librement adapté au sein du laboratoire et complété par les renseignements cliniques qui sont normalement demandés.
Conseil intégré/conjoint
- Q : À partir de l’âge de 60 ans, le conseil standard (selon le tableau des conseils intégrés/conjoint, annexe 1) doit-il toujours être donné en cas de résultat négatif pour le hrHPV, à savoir « Intervalle de dépistage normal (répétition dans 5 ans) » ?
-
R : Dans le tableau du conseil intégré, une limite d’âge est ajoutée à ce résultat : <60 ans. En outre, une note de bas de page indique qu’à partir de 60 ans, le conseil « aucun suivi supplémentaire n’est indiqué dans le cadre du dépistage organisé » peut être donné en cas de résultat hrHPV négatif.
(Applicable à la fois au dépistage primaire et au deuxième triage après 12 mois).
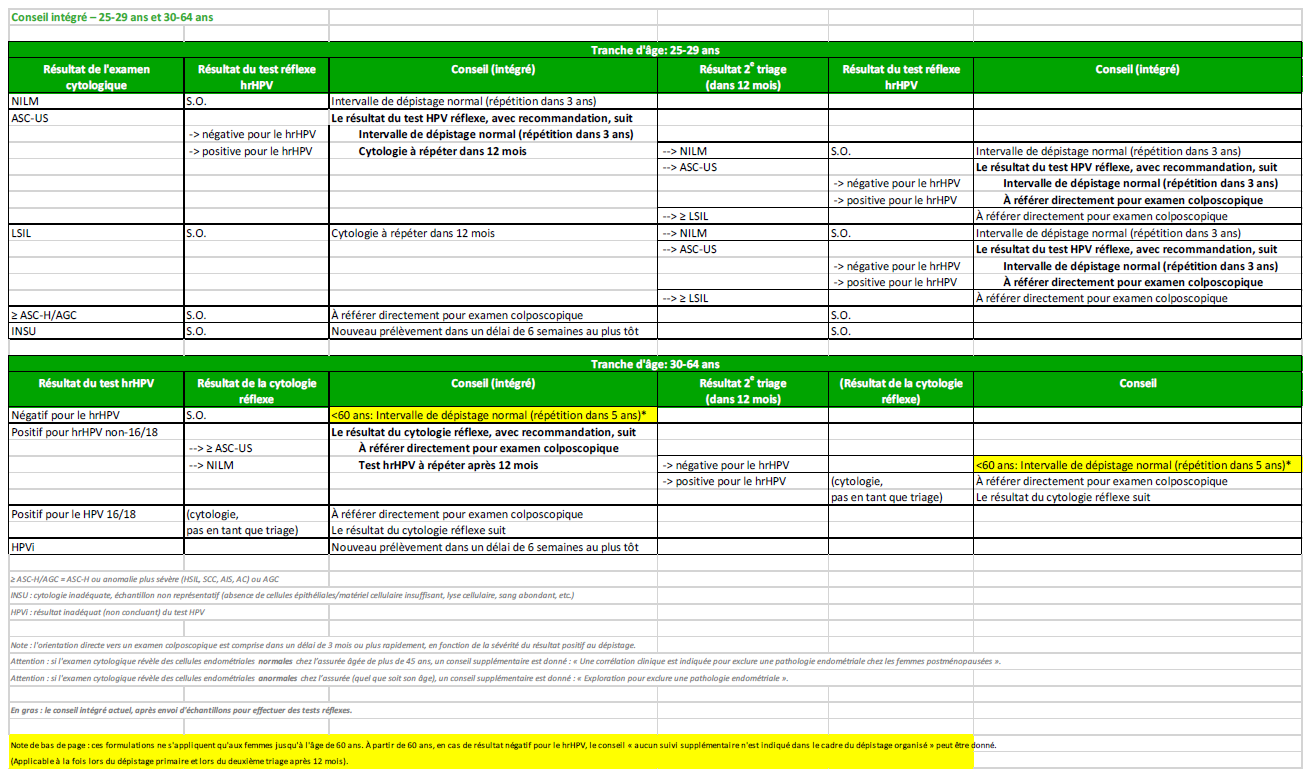
Note de bas de page : ces formulations ne s’appliquent qu’aux femmes jusqu’à l’âge de 60 ans. À partir de 60 ans, en cas de résultat négatif pour le hrHPV, le conseil « aucun suivi supplémentaire n’est indiqué dans le cadre du dépistage organisé » peut être donné.(Applicable à la fois lors du dépistage primaire et lors du deuxième triage après 12 mois).
- Q : Échantillons d’HPV avec l’indication « suivi (diagnostique/thérapeutique) » : le laboratoire ne dispose souvent pas des données complètes sur les antécédents cliniques; quels sont les conseils à donner ?
-
R : Dans la nomenclature, un conseil n’est demandé que pour le dépistage, pas pour les échantillons de suivi, car l’avis dépend des antécédents du patient. Il incombe donc au médecin traitant (qui dispose de ces données) de tirer des conclusions des résultats de laboratoire pour ce processus pathologique.
- Q : Faut-il envoyer un conseil pour les échantillons de HPV demandés « hors indication » ?
-
R : Le laboratoire ne doit pas fournir un conseil dans ce cas, uniquement pour l’indication «dépistage». Pour les tests hors indication, il incombe au médecin demandeur d’assurer un suivi correct.
- Q : En ce qui concerne le conseil à fournir par le « prestataire de cytologie primaire » : ce prestataire doit-il incorporer l’ensemble du rapport HPV, une partie de celui-ci ou seulement la conclusion dans le conseil ? Ou bien le prestataire de soins de santé n’est-il pas tenu de le faire ?
-
R : La nomenclature ne contient aucune exigence formelle à ce sujet. Les résultats ou les conclusions d’autres services ne doivent pas être mentionnés.
Un conseil intégré/conjoint doit être donné pour un dépistage primaire suivi d’un test réflexe, avec le libellé figurant dans l’annexe 1 de la directive scientifique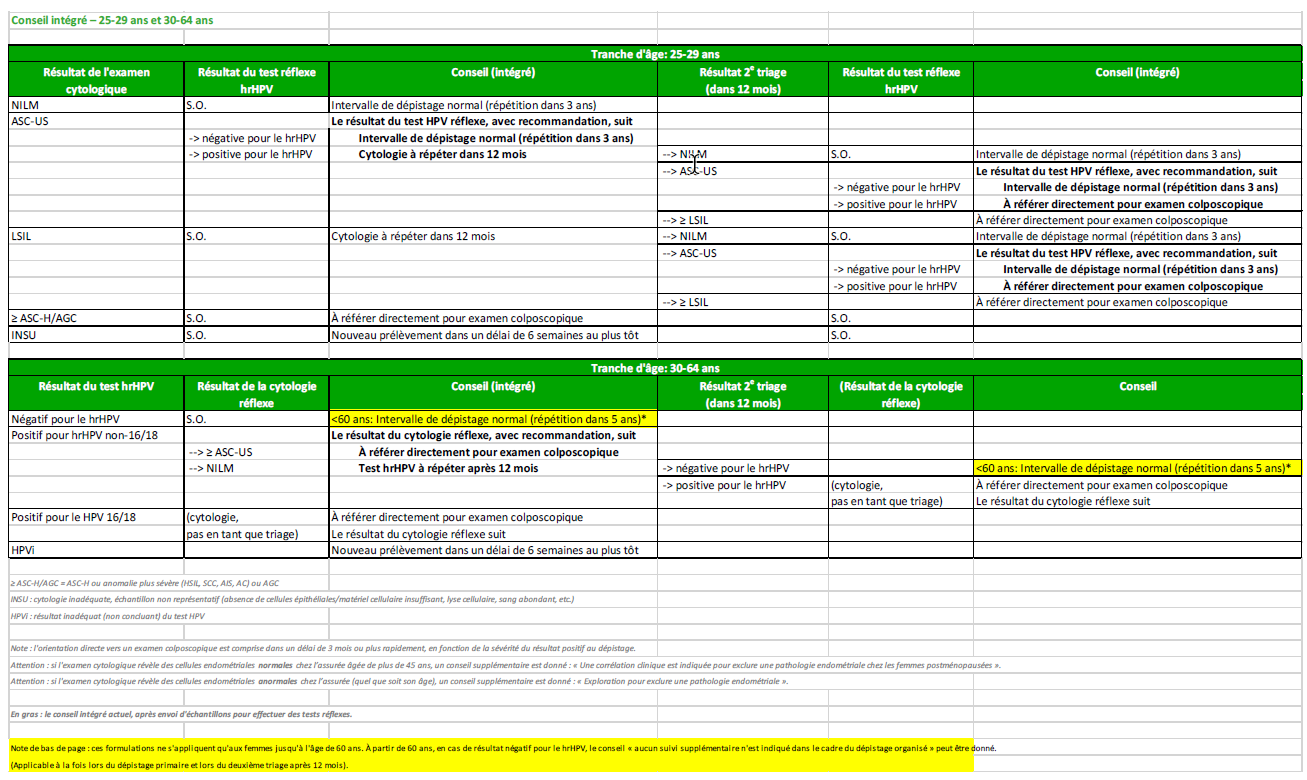
Enregistrement auprès BCR (La Fondation Régistre du Cancer)
- Q : Lorsque le médecin/la patiente insiste pour effectuer un test HPV en dehors du programme de dépistage standard, le résultat de ce test HPV doit-il être communiqué au BCR ?
-
R : Les résultats des dépistages remboursés doivent être obligatoirement enregistrés, conformément à l’article 5, point a), de l’article 24 bis de la nomenclature. En outre, tous les résultats des tests HPV et de cytologie pour tous les échantillons du col de l’utérus (et pas seulement dans le contexte du dépistage du cancer du col de l’utérus) doivent être communiqués au BCR.
(Les laboratoires d’anatomie pathologique ainsi que les laboratoires de biologie clinique sont légalement tenus d’enregistrer les données relatives aux résultats du diagnostic précoce du cancer auprès de la Fondation Régistre du Cancer (Belgian Cancer Registry, BCR)1. La loi fournit ainsi une base légale au BCR pour collecter des données sur les échantillons du col de l’utérus et les inclure dans son registre cyto-histo-pathologique.) - Q : Seuls les échantillons prélevés au niveau du col de l’utérus doivent-ils être enregistrés au BCR ? En d’autres termes, les résultats des échantillons prélevés sur un autre site d’échantillonnage (paroi vaginale, dôme vaginal, vulve) sont-ils exclus de la rapportage au BCR ?
-
R : Tant les laboratoires d’anatomie pathologique que les laboratoires de biologie clinique ont l’obligation légale d’enregistrer les données relatives à leurs résultats concernant la détection précoce du cancer auprès du Registre belge du cancer (RBC).1 Il existe donc une base légale permettant au BCR de collecter des données sur les échantillons prélevés sur le col de l’utérus et de les inclure dans le registre de cyto-histo-pathologie.
En outre, tous les échantillons liés à un diagnostic oncologique doivent être envoyés au BCR. Cela comprend les résections de la tumeur primaire et des métastases, les examens diagnostiques, les deuxièmes opérations (y compris les marges sans tumeur), les échantillons négatifs liés à une tumeur connue et les examens complémentaires.
Les échantillons du dôme vaginal prélevés dans le cadre du suivi après une hystérectomie, à la suite d’un cancer du col de l’utérus in situ ou invasif, doivent également être déclarés au BCR. Il s’agit alors d’un suivi. Les retraits du dôme vaginal après hystérectomie pour d’autres raisons non oncologiques ne doivent pas être rapportés au BCR car ils sortent du cadre du dépistage.
Nieuwsbrieven | Belgian Cancer Registry / Bulletins d’information | Belgian Cancer Registry
Opvragingsronde | Belgian Cancer Registry / En général | Belgian Cancer Registry
[1] Art. 138, §2, 3°, a) Loi coordonnée du 10 mai 2015 relative à l’exercice des professions des soins de santé, M. B. 18 juin 2015.
Pour les laboratoires d’anatomie pathologique, cette exigence d’enregistrement est également intégrée dans leurs normes d’agrément: art. 35, 6° Arrêté royal du 5 décembre 2011 relatif à l’agrément des laboratoires d’anatomie pathologique par le Ministre qui a la Santé publique dans ses attributions, M. B. 13 février 2012.
Retour à la page screening cancer du col de l’utérus
Lire la directive scientifique


