Veelgestelde vragen rond de introductie van de HPV-test in baarmoederhalskanker screening in België
- Voor specifieke vragen ivm de NOMENCLATUUR (codes, terugbetaling, notificatie, …): Primaire screening van baarmoederhalskanker met HPV | RIZIV
- Voor technische vragen ivm HPV-TESTEN: zie ‘Veelgestelde vragen’ Nationaal Referentiecentrum (NRC) voor Humaan papillomavirus | sciensano.be
- Voor specifieke vragen ivm REGISTRATIE: Nieuwsbrieven | Belgian Cancer Registry / Opvragingsronde | Belgian Cancer Registry
Algemeen
- V : Wat moeten we doen met de aanbevelingen die in 2024 zijn gegeven voor diagnostische opvolging (hertesting na 6 maanden in plaats van de nieuwe aanbeveling na 1 jaar)?
-
A : Rechthebbenden van wie de screening in 2024 positief was en die de oude aanbeveling kregen, kunnen de voorgestelde opvolging voortzetten. Ze zullen een terugbetaald opvolguitstrijkje krijgen na 6 maanden in plaats van de 12 maanden die nu voorzien is in het nieuwe algoritme (in 2025), maar slechts één vergoeding per kalenderjaar. Na deze terugbetaalde diagnostische opvolging (op 6 maanden) zal het advies gegeven worden volgens de nieuwe screeningsschema’s; m.a.w. worden doorverwezen voor routinescreening of colposcopie — afhankelijk van de resultaten van de test(en). De opvolgtest moet in overeenstemming zijn met de nieuwe screeningsalgoritmen: cytologie voor 25-29-jarigen, een HPV-test voor 30-64-jarigen.
- V : Indien een patiënt een afwijkend screeningsresultaat heeft, maar bij de 12 maanden opvolging (2de triage) terugkeert naar het normale screeningsschema, is de volgende screening dan 3 of 4 jaar na de initiële screening?
-
A : De volgende screening voor rechthebbenden na een initieel afwijkend screeningsresultaat, maar met een negatief 2de triage resultaat (opvolging na 12 maanden), is effectief 3 jaar( voor cytologie) of 5 jaar (voor een HPV-test) na het laatste negatieve testresultaat. Dit betekent dus effectief 4 jaar (voor cytologie) of 6 jaar (voor een HPV-test) na het initiële screeningsresultaat.
(In Vlaanderen zal CvKO uitnodigingsbrieven versturen en de rechthebbende op correcte wijze informeren wanneer er opnieuw gescreend dient te worden.)
- V : Hoe dient bij een patiënt met een positieve primaire HPV-test die — conform de Sciensano richtlijn — een opvolgtest na 12 maanden vereist (2de triage), het tijdstip gekozen te worden voor deze opvolgtest, zodat de patiënt zeker is van terugbetaling? Is dit (ten vroegste) na 1 kalenderjaar, of is er eventueel een welbepaald tijdsinterval dat gehanteerd dient te worden?
-
A : ‘Na 12 maanden’ betekent hier letterlijk ten vroegste na een interval van 1 jaar. Best niet vroeger, gezien de tijd die nodig is om een HPV infectie te klaren en eventuele regressie van het letsel toe te laten, maar we begrijpen ook dat het inplannen van opvolgonderzoeken niet dag op dag 12 maanden later kan gebeuren. Er werd geopteerd om hier geen welbepaald interval te definiëren, maar dit over te laten aan een goede praktijkvoering. Er is dus zeker geen twijfel over terugbetaling voor de patiënt indien dit net binnen 12 maanden valt (met voorkeur voor een iets ruimere periode dan 12 maanden gezien bovenstaande) of eventueel zelfs met een paar weken/maanden vertraging ingepland wordt.
- V : Hoe moet de opvolging na hysterectomie voor neoplastische letsels van de baarmoederhals (plaveiselcelcarcinoom of adenocarcinoom) gebeuren?
-
A : De opvolging van patiënten met baarmoederhalskanker (adeno en squameus) is zeer gevarieerd. De opvolgingsstrategieën verschillen van ziekenhuis tot ziekenhuis; ook de internationale richtlijnen verschillen. Cytologie is niet de standaard voor opvolging, maar wordt in sommige ziekenhuizen wel gebruikt. Hetzelfde geldt voor PET-scans en tumormarkers. Daarom zijn er nog geen Belgische richtlijnen opgesteld.
Het is steeds mogelijk om op te volgen onder indicatie ‘(therapeutische) opvolging’.
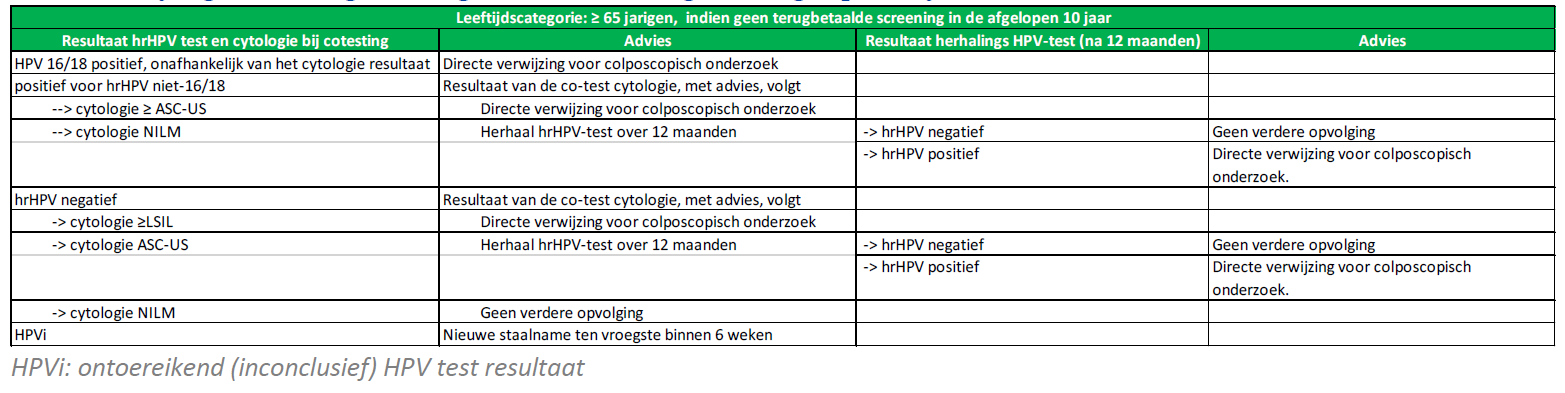
- V : Bij 65+ : na de 12 maanden opvolging (2de triage), gedurende hoeveel jaar wordt de follow-up vergoed?
-
A : Opvolging staat los van de leeftijd. Er is steeds maar één opvolging (na 12 maanden, de 2de triage stap) die resulteert in een definitief klinisch advies voor de 65+ groep, evenals de jongere doelgroep, en er zou geen verdere (jaarlijkse) opvolging nodig moeten zijn (behalve bij opvolging van een bewezen hrHPV infectie (postcolposcopie), opvolging na behandeling van CIN 2+, en dit zolang opvolging noodzakelijk is volgens de wetenschappelijke richtlijn).
-
V : Er is discordantie tussen de nomenclatuur en de Sciensano richtlijn voor wat betreft de uit te voeren onderzoeken bij screening van hoogrisicogroepen. In de nomenclatuur staat hrHPV EN cytologie gedefinieerd (553674-553685 voor hrHPV en 591835-591846 voor cytologie). In de Sciensano richtlijn daarentegen wordt er een onderscheid gemaakt tussen:
DES/AIS: co-testing VS Immuungecompromiteerde patiënten: hrHPV OF cytologie ifv de leeftijd (dit is zo niet opgenomen in de nomenclatuur, volgens de nomenclatuur is het hier ook co-testing) -
Cotesting bij DES/AIS is ten alle tijden correct.
Voor immuungecompromitteerde patiënten:volgens de nomenclatuur - gezien dit een hoogrisicogroep is — zou een co-test (gelijktijdige HPV-test en cytologie) terugbetaald worden, maar de ‘wetenschappelijke richtlijn’ schrijft cytologie OF een HPV-test voor. De experten hebben immers uitgemaakt dat een co-test niet vereist is bij immuungecompromitteerde patiënten. In de ‘wetenschappelijke richtlijn’ vind je de screening algoritmes voor immuungecompromitteerde jonge patienten (21-29 jaar) en ouderen (30+) terug. Hier zie je dat voor de jongeren jaarlijkse cytologie wordt aanbevolen en voor de 30+ een 3-jaarlijkse HPV-test. Co-testing werd dus niet als de meest optimale test aanschouwd in deze indicaties.
De ‘wetenschappelijke richtlijn’ vermeldt verder:
Eén en dezelfde nomenclatuurcode wordt voorzien voor testen bij hoogrisicogroepen en testen bij klinische indicaties (591835-591846 voor cytologie en 553674-553685 voor HPV-testen), zonder leeftijdsbeperking. Er wordt echter een door experten overeengekomen testfrequentie aanbevolen (zie 3.3-3.4). Het is de verantwoordelijkheid van de behandelende arts om de aanbevolen testfrequentie met de aangerade test op te volgen (cotesting bij DES/AIS en HPV-test of cytologie bij immuungecompromitteerde groepen, afhankelijk van de leeftijd).
- V : Patiënten die vallen onder de categorie hoogrisico (bv. DES of immuunsuppressie), stopt bij hen de screening ook op 65 jaar of gaat dit levenslang (of zolang de immuunsuppressieve behandeling voortduurt) verder?
-
A : Voor hoogrisico groepen staat er geen leeftijdslimiet op de testmogelijkheden. Testen kan zodra en zolang medisch gezien noodzakelijk is.
-
V : Patiënten die een conisatie gehad hebben, moeten na 2x negatieve HPV-test zich verder 3-jaarlijks laten screenen gedurende 25 jaar en nadien terug 5-jaarlijks.
a) Hoe dient die 3-jaarlijkse HPV-test aangerekend te worden? b) Als hier een positief HPV-resultaat verkregen wordt, dient er dan automatisch een reflexcytologie te gebeuren in het labo. -
A: a) Aanrekening via 149634-149645 voor de afname van een opvolguitstrijkje, voor de HPV-test die hierop wordt uitgevoerd is dat 553652-553663.
b) Reflexcytologie dient in opvolging (post-colposcopisch) automatisch te gebeuren bij een positief HPV resultaat.
- V : In gevallen van eerdere abnormale cytologie met een negatieve HPV PCR (vb. LSIL — HPV negatief in 2023) wordt in 2025 alleen een PCR aangevraagd en deze is negatief. Moet het labo dan een (reflex)cytologie toevoegen?
-
A : Neen, er volgt geen reflextest na een negatief primair testresultaat. Bovendien moet een HPV-test niet worden uitgevoerd op LSIL-gevallen (in het nieuwe screeningsalgoritme), omdat het geen relevante informatie toevoegt voor de opvolging of behandeling van de vrouw. Na 12 maanden dient een opvolg-cytologie (2de triage) te worden aangevraagd, met als eindpunt ‘terug verwijzing naar de routine screening’ (indien NILM of ASC-US/HPV negatief) of ‘colposcopie’ (indien ASC-US/HPV positief of >=LSIL).
Echter, in uitzondering voor resultaten verkregen vóór 2025 vermeld hoofdstuk 4 van de wetenschappelijke richtlijn:
4.2. HPV-negatieve ASC-US/LSIL (screeningsresultaten verkregen vóór 2025)
- hrHPV-negatieve LSIL
Vrouwen met een LSIL-testresultaat moeten niet worden doorverwezen voor een HPV-test, maar in het zeldzame geval dat er in het vorige screeningsprogramma co-testing (simultane HPV-test en cytologie) uitgevoerd is, moeten deze vrouwen na 12 maanden opnieuw worden getest op HPV.- Als het resultaat van de nieuwe test hrHPV-negatief is, kan de vrouw veilig worden doorverwezen naar routinescreening.
- Als de nieuwe HPV-test hrHPV-positief is, moet de vrouw worden doorverwezen voor een onmiddellijke colposcopie, gezien het 5-jaars risico op CIN3+ rond 2,0% uitkomt (27).
- hrHPV-negatieve LSIL
- V : Is er een voorbeeld aanvraagformulier beschikbaar voor de cervicovaginale cytologie en HPV-test binnen het nieuwe baarmoederhalskanker screenings programma?
-
A : Ja, er werd een voorbeeld als suggestie uitgewerkt dat alle mogelijkheden binnen het nieuwe screeningsprogramma afdekt. Dit is vrij aan te passen binnen het labo en aan te vullen met de klinische inlichtingen die normaal bevraagd worden.

Geïntegreerd / gezamenlijk advies
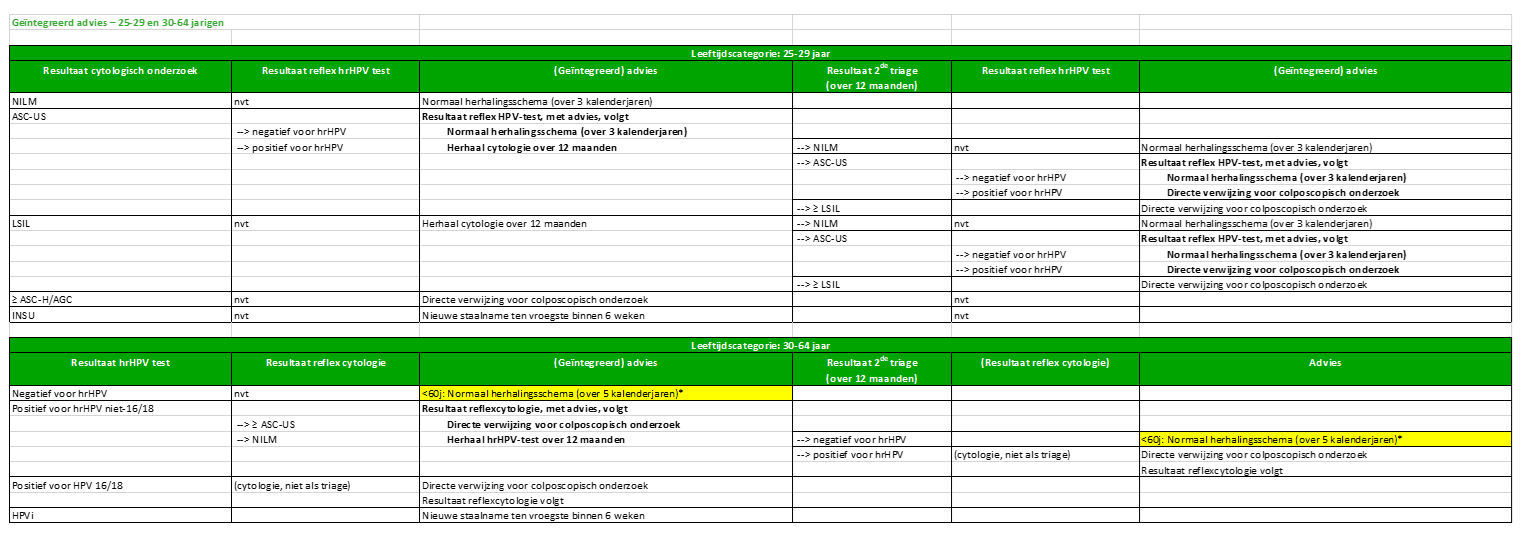
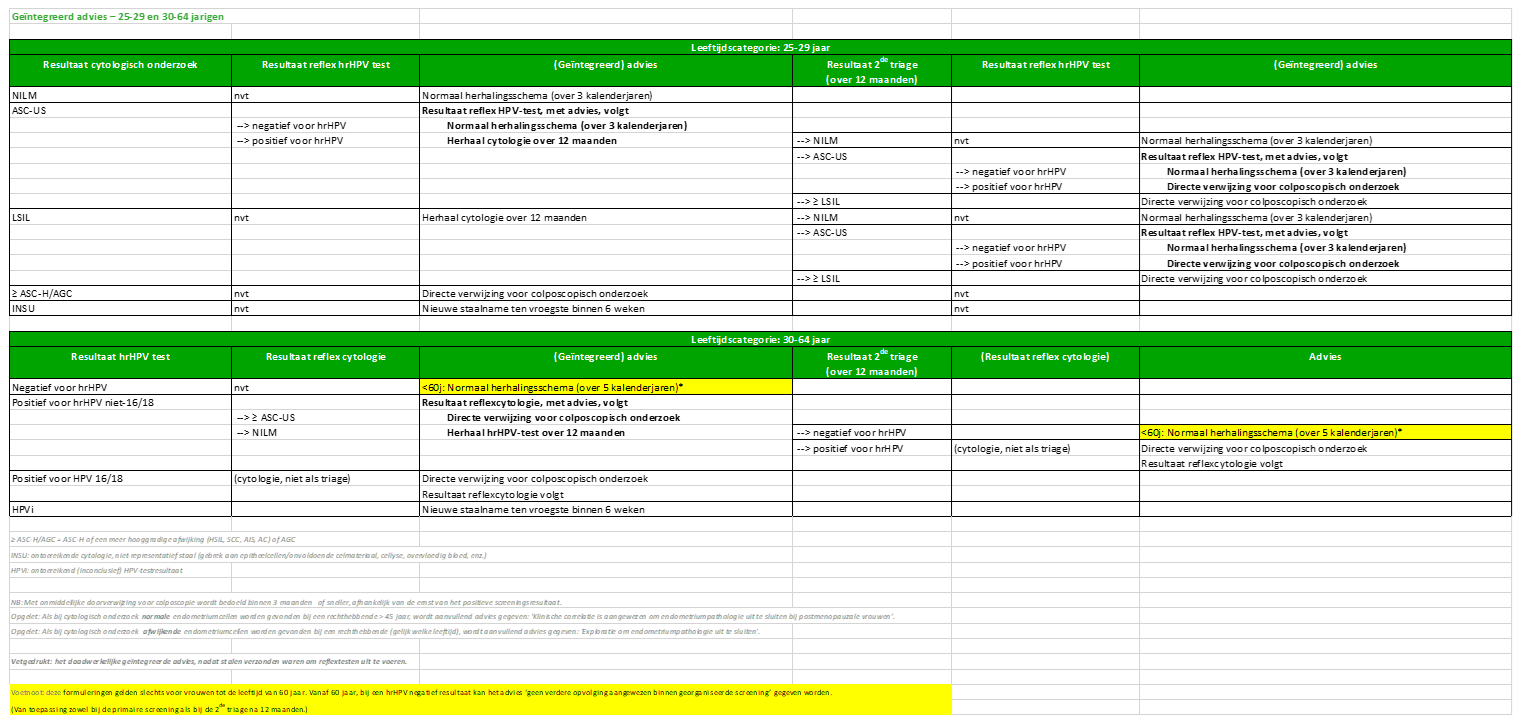
- V : Dient vanaf de leeftijd van 60 jaar nog steeds het standaard advies (volgens tabel geïntegreerd/gezamenlijk advies, annex 1) gegeven te worden bij een hrHPV-negatief resultaat, mn. “normaal herhalingsschema (over 5 kalenderjaren)”?
-
A : In de tabel van het geïntegreerd advies wordt bij dit resultaat een leeftijdslimiet toegevoegd: <60 jaar. Verder wordt in een voetnoot aangegeven dat vanaf 60 jaar bij een hrHPV-negatief resultaat het advies ‘geen verdere opvolging aangewezen binnen georganiseerde screening’ kan gegeven worden. (Van toepassing zowel bij de primaire screening als bij de 2de triage na 12 maanden.)
Voetnoot: deze formuleringen gelden slechts voor vrouwen tot de leeftijd van 60 jaar. Vanaf 60 jaar, bij een hrHPV negatief resultaat kan het advies ‘geen verdere opvolging aangewezen binnen georganiseerde screening’ gegeven worden.
(Van toepassing zowel bij de primaire screening als bij de 2de triage na 12 maanden.)
- V : HPV stalen met als indicatie “opvolging (diagnostisch/therapeutisch)”: er zijn vaak geen volledige klinische gegevens van de voorgeschiedenis beschikbaar voor het labo, welk advies dient er gegeven te worden?
-
A : In de nomenclatuur wordt enkel een advies gevraagd bij screening, niet voor opvolgstalen, gezien het advies afhankelijk is van de voorgeschiedenis van de patiënt. Het is dus de verantwoordelijk van de aanvragende arts (die deze gegevens ter beschikking heeft) om voor dit ziekteproces conclusies te trekken uit de laboresultaten.
- V : Dient er een advies meegestuurd te worden voor HPV stalen gevraagd “buiten indicatie”?
-
A : Er dient in deze omstandigheid geen advies te worden gegeven vanuit het labo, enkel voor de indicatie ‘screening’. Voor testen buiten indicatie is het de verantwoordelijkheid van de aanvragende arts om de correcte opvolging te garanderen.
- V : Betreffende de aanbeveling die de “zorgverlener van de primaire cytologie moet verstrekken”: moet deze zorgverlener het volledige HPV rapport of een deel ervan of enkel de conclusie in de aanbeveling incorporeren? Of heeft de zorgverlening hier geen verplichting toe?
-
A : Er wordt in de nomenclatuur geen vorm-eis gesteld hierover, resultaten of besluiten van andere prestaties moeten niet vermeld worden. Er dient bij primaire screening gevolgd door reflex-testing een geïntegreerd (gezamenlijk) advies gegeven te worden, met de formuleringen zoals die terug te vinden zijn in annex 1 van de wetenschappelijke richtlijn:
Rapportering aan BCR (Stichting Kankerregister)
- V : Wanneer de arts/patiënt aandringt op de uitvoering van een HPV-test buiten het standaard screeningsschema, dient het resultaat van deze HPV-test dan gerapporteerd te worden aan BCR?
-
A : Terugbetaalde screeningsresultaten moeten verplicht geregistreerd worden, overeenkomstig artikel 5a) van artikel 24bis van de nomenclatuur. Bovendien dienen alle HPV en cytologie resultaten voor alle cervicale stalen (niet enkel in het kader van baarmoederhalskankerscreening) gerapporteerd te worden aan BCR.
(Zowel de laboratoria voor pathologische anatomie als de laboratoria voor klinische biologie hebben de wettelijke verplichting om gegevens over hun resultaten met betrekking tot de vroegopsporing van kanker te registreren bij de Stichting Kankerregister (Belgian Cancer Registry, BCR)1. Er bestaat daardoor een wettelijke basis voor BCR om gegevens over stalen van de baarmoederhals te verzamelen en op te nemen in het cyto-histo-pathologieregister.) - V : Moeten enkel stalen afgenomen ter hoogte van de cervix gerapporteerd worden aan BCR? Met andere woorden zijn resultaten van stalen afgenomen op een alternatieve afnameplaats (vaginawand, vaginakoepel, vulva) uitgesloten voor rapportage aan BCR?
-
A : Zowel de laboratoria voor pathologische anatomie als de laboratoria voor klinische biologie hebben de wettelijke verplichting om gegevens over hun resultaten met betrekking tot de vroegopsporing van kanker te registreren bij de Stichting Kankerregister (Belgian Cancer Registry, BCR)1. Er bestaat daardoor een wettelijke basis voor BCR om gegevens over stalen van de baarmoederhals te verzamelen en op te nemen in het cyto-histo-pathologieregister.
Daarnaast moeten alle stalen met betrekking tot een oncologische diagnose naar BCR verstuurd worden. Dit omvat resecties van zowel de primaire tumor als metastasen, diagnostische onderzoeken, tweede ingrepen (inclusief tumorvrije marges), negatieve stalen gerelateerd aan een gekende tumor en aanvullende onderzoeken.
Stalen van de vaginakoepel afgenomen in opvolging na hysterectomie, n.a.v. een in situ of invasieve tumor baarmoederhalskanker, dienen ook gerapporteerd te worden aan BCR. Dat is dan in het kader van opvolging. Afnames van de vaginakoepel na hysterectomie voor andere, niet-oncologische redenen moeten niet gerapporteerd worden aan BCR omdat deze buiten de scope van screening vallen.
Nieuwsbrieven | Belgian Cancer Registry / Bulletins d’information | Belgian Cancer Registry
Opvragingsronde | Belgian Cancer Registry / En général | Belgian Cancer Registry
[1] Art. 138, §2, 3°, a) Gecoördineerde Wet van 10 mei 2015 op de uitoefening van de gezondheidszorgberoepen, B.S. 18 juni 2015.
Voor de laboratoria voor pathologische anatomie is deze registratieverplichting ook opgenomen in de erkenningsregels: art. 35, 6° Koninklijk Besluit van 5 december 2011 betreffende de erkenning van de laboratoria voor pathologische anatomie door de Minister tot wiens bevoegdheid de Volksgezondheid behoort, B.S. 13 februari 2012.
Terug naar baarmoederhalskanker screening
Lees de volledige klinische toelichting