Algemene info voor zorgverleners ivm de nieuwe baarmoederhalskankerscreening in België
In december 2022 besliste de Interministeriële Conferentie (IMC) Volksgezondheid (in lijn met eerdere beslissingen van de IMC tijdens de vorige regeerperiode), om voor baarmoederhalskanker screening over te schakelen van cytologie naar HPV-testing (vanaf de leeftijd van 30 jaar). Deze beslissing is gebaseerd op beschikbare wetenschappelijke evidentie, gaande van het KCE-rapport 238 uit 2015 tot zeer recente analyses van de Wereldgezondheidsorganisatie (WGO) en het Internationaal Agentschap voor Kankeronderzoek (IARC). De wijziging werd van kracht op 1 januari 2025.
Op deze webpagina vindt u een overzicht van de informatie die werd verzameld door alle bijdragende actoren (samen met hun respectievelijke websites) over de volgende onderwerpen;
- de klinische toelichting bij de nieuwe screeningsalgoritmes,
- de wijzigingen in de nomenclatuur en de terugbetalingsregels,
- de bijzondere bepalingen voor de accreditatie van medische laboratoria,
- de lijst van goedgekeurde HPV-testen,
- de regelgeving voor de registratie van screeningsresultaten, en
- belangrijke implicaties voor de laboratoria
1. Klinische toelichting voor de zorgverleners
In samenwerking met VVOG en Domus Medica ondersteund door de Commissies Klinische Biologie en Pathologische Anatomie
Lees het volledige document van de wetenschappelijke richtlijn
De klinische toelichting voor zorgverleners bevat informatie over de nieuwe testschema’s, het geïntegreerd advies, het notificatie formulier en andere essentiële details, waarbij een onderscheid wordt gemaakt tussen immuungecompromitteerde patiënten en de algemene bevolking en waarbij individuen worden ingedeeld naar leeftijdsgroep.
ALGEMENE BEVOLKING
- Voor alle : primaire screening & reflextesten (triage) — Nieuw test schema
-
tabel 1. nieuw test schema: primaire screening & reflextesten (triage) (hoofdstuk 2.2.)

1 Indien de afgelopen 10jaar geen screening werd terug betaald.
OPMERKING: Binnen de primaire screening (25-64j) is er geen plaats — en is er geen terugbetaling voorzien — voor een co-test (een gecombineerde HPV-test en cytologie) aangezien de meerwaarde wetenschappelijk niet werd aangetoond.
Meer infomatie in het document van de
 wetenschappelijke richtlijn hoofdstuk 2.2
wetenschappelijke richtlijn hoofdstuk 2.2 Lees het volledige document van de wetenschappelijke richtlijn
-
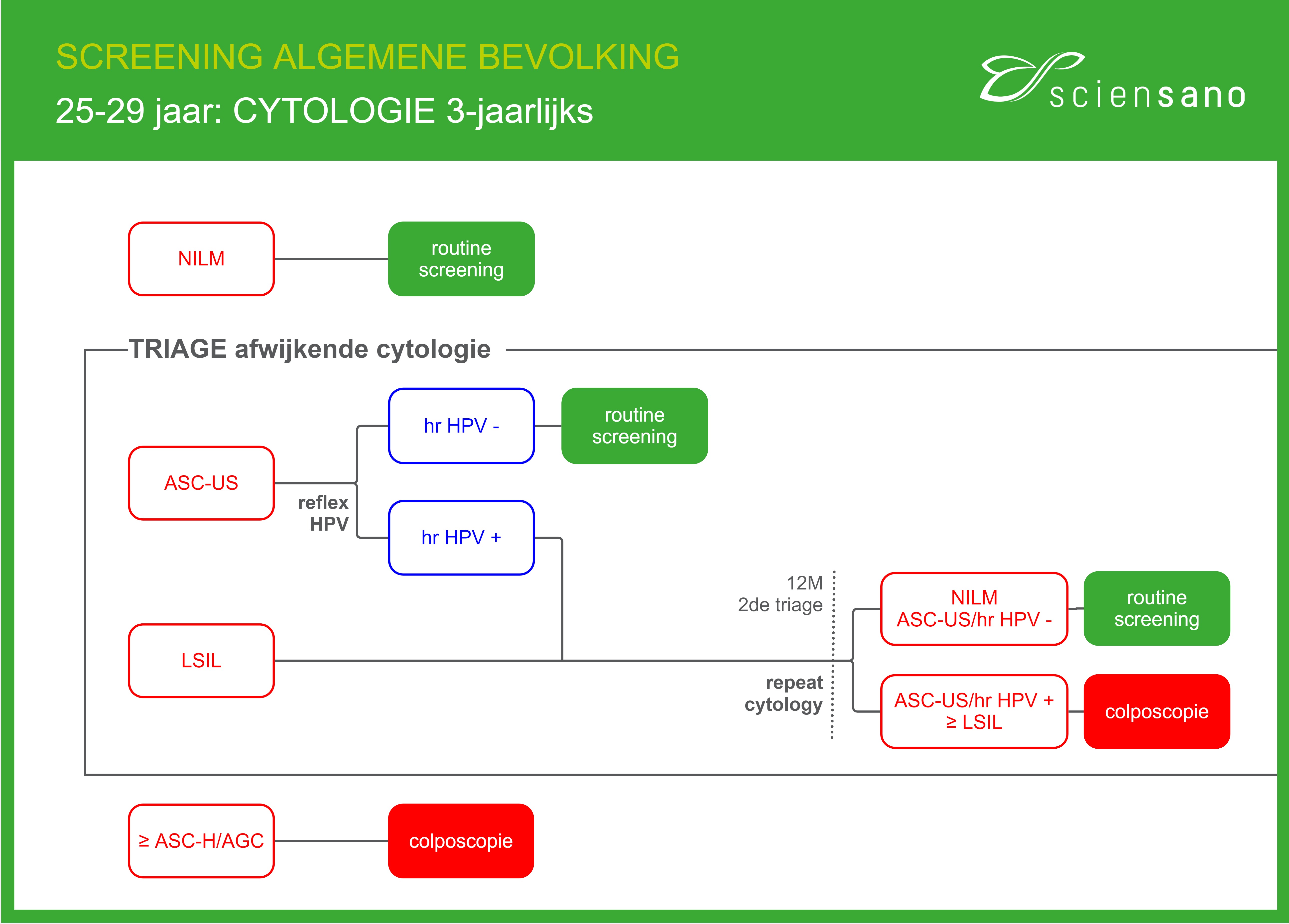
25-29 jaar : primaire screening, reflextesten (triage) en opvolging in de algemene bevolking (Nieuw screeningsalgoritme)
-
figuur 1. Screeningalgoritme voor 25-29-jarigen, in de algemene bevolking (hoofdstuk 2.3.)
Meer infomatie in het document van de
 wetenschappelijke richtlijn hoofdstuk 2.3.
wetenschappelijke richtlijn hoofdstuk 2.3.Lees het volledige document van de wetenschappelijke richtlijn
- 30-64 year : primaire screening, reflextesten (triage) en opvolging in de algemene bevolking (Nieuw screeningsalgoritme)
-
figuur 2. Screeningalgoritme voor 30-60-jarigen, in de algemene bevolking (hoofdstuk 2.3.)

Meer infomatie in het document van de
 wetenschappelijke richtlijn hoofdstuk 2.3.
wetenschappelijke richtlijn hoofdstuk 2.3.Lees het volledige document van de wetenschappelijke richtlijn
IMMUUNGECOMPROMITTEERDE PATIËNTEN
+ opvolging/klinische testen/hoogrisicogroepen
- Voor allen : opvolging, klinische testen (bij symptomen), en hoogrisicogroepen (Nieuw testschema)
-
tabel 2. nieuw testschema : opvolging, klinische testen (bij symptomen), en hoogrisicogroepen (hoofdstuk 3.1.)
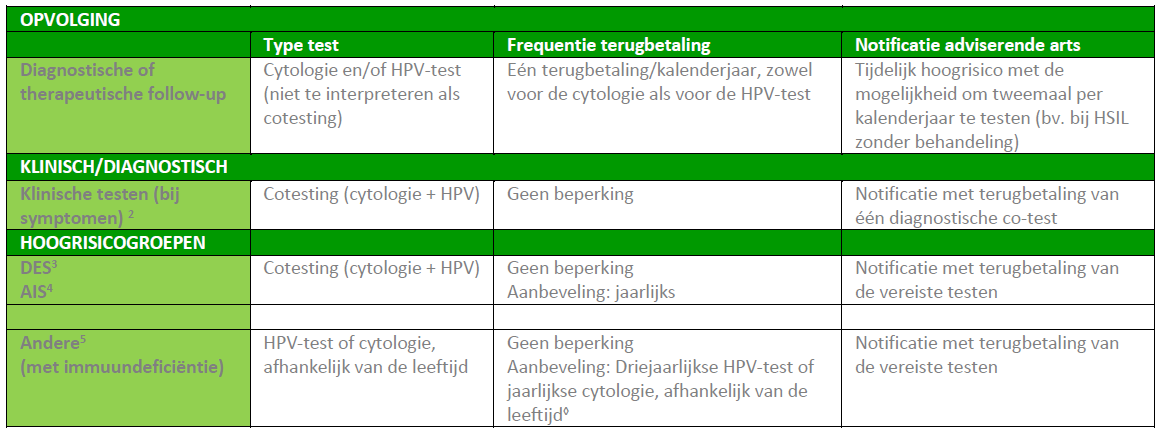
2 Indicaties: postmenopauzaal bloedverlies, abnormaal therapieresistent vaginaal bloedverlies, onverklaard post-coïtaal bloedverlies
3 DES = diethylstilbestrol: synthetisch oestrogeen dat tussen 1938 en 1971 werd voorgeschreven aan zwangere vrouwen om een miskraam te voorkomen. De dochters van de met DES-behandelde vrouwen hebben een verhoogd risico op kankers, waaronder baarmoederhalskanker
4 AIS = adenocarcinoma in situ
5 BIJGEWERKTE DEFINITIE vs. nomenclatuur: bij alle patiënten met immuunsuppressie (hiv-positieve patiënten (CD4 <350/µl of HIV RNA > 200 cp/ml), na orgaantransplantatie, na allogene stamceltransplantatie, systemische lupus erythematosus, congenitale primaire immuundeficiëntie, of patiënten die langdurig aanhoudende immuuunsuppressiva krijgen) is frequentere screening vereist zolang de immuunsuppressieve behandeling duurtMeer infomatie in het document van de
 wetenschappelijke richtlijn hoofdstuk 3.1
wetenschappelijke richtlijn hoofdstuk 3.1Lees het volledige document van de wetenschappelijke richtlijn
- 21-29 jaar : primaire screening, reflextesten (triage) en opvolging in immuungecompromitteerde patiënten (Nieuw screeningsalgoritme)
-
figuur 3. Screeningsalgoritme voor 21-29-jarigen, in immuungecompromitteerde patiënten (hoofdstuk 3.4.)

Meer infomatie in het document van de
 wetenschappelijke richtlijn 3.4.
wetenschappelijke richtlijn 3.4.Lees het volledige document van de wetenschappelijke richtlijn
- >30 year : primaire screening, reflextesten (triage) en opvolging in immuungecompromitteerde patiënten (Nieuw screeningsalgoritme)
-
figuur 4. Screeningsalgoritme voor ≥30-jarigen, in een immungecompromitteerde patiënten (hoofdstuk 3.4.)

Meer infomatie in het document van de
 wetenschappelijke richtlijn hoofdstuk 3.4.
wetenschappelijke richtlijn hoofdstuk 3.4.Lees het volledige document van de wetenschappelijke richtlijn
ALGEMENE INFORMATIE
- Klinische toelichting
-
Het wetenschappelijk advies rond de therapeutische opvolging :
 wetenschappelijke richtlijn hoofdstuk 5. (gevalideerd door Sciensano in consensus met de betrokken beroeps- en wetenschappelijke verenigingen)
wetenschappelijke richtlijn hoofdstuk 5. (gevalideerd door Sciensano in consensus met de betrokken beroeps- en wetenschappelijke verenigingen)He kwaliteitsrichtlijnen colposcopie met voorbeeld-sjabloon van het gestandardiseerd verslag voor colposcopie:
 wetenschappelijke richtlijn hoofdstuk 6.
wetenschappelijke richtlijn hoofdstuk 6.Lees het volledige document van de wetenschappelijke richtlijn
- Notificatie formulier
-
Praktische aspecten
Download hier het notificatie fomulier: https://www.riziv.fgov.be/SiteCollectionDocuments/formulier-notificatie-baarmoederhalsscreening.pdf
Het is de verantwoordelijkheid van de behandelende arts om het notificatieformulier correct en volledig in te vullen. Dit papieren formulier (zie hierboven) moet per post* naar het ziekenfonds (mutualiteit) van de patiënt worden verzonden. Na ontvangst van het formulier registreert het ziekenfonds de patiënt, zodat deze van bijkomende terugbetalingen kan genieten. De controlerende geneesheer geeft dus geen goedkeuring, het gaat enkel om een kennisgeving (en niet om een aanvraag tot goedkeuring).
Het INAMI kan het aantal meldingen voor hoogrisicogroepen (inclusief tijdelijk hoogrisico) en voor klinische episodes controleren, eventuele misbruiken opsporen en gepaste maatregelen nemen.
Het laboratorium krijgt geen ontvangstbevestiging van het ziekenfonds en kan dus niet weten of de bevestiging geregistreerd is en of de bijkomende terugbetaling zal plaatsvinden. Weigering van terugbetalingen door het ziekenfonds moet daarom in eerste instantie besproken worden met de aanvragende arts die verantwoordelijk is voor dit proces
De pseudocodes op het notificatieformulier zijn uitsluitend bestemd voor intern gebruik door het RIZIV.
* De adressen van de ziekenfondsen kunnen hier eenvoudig teruggevonden worden: https://www.riziv.fgov.be/nl/professionals/andere-professionals/ziekenfondsen/contacteer-de-ziekenfondsen
Meer infomatie in het document van de
 wetenschappelijke richtlijn hoofdstuk 3.5.
wetenschappelijke richtlijn hoofdstuk 3.5. - Samenwerkende partners
-
Meer informatie op de website van onze samenwerkende partners:
2. Nomenclatuur en terugbetalingen
In samenwerking met RIZIV
Koninklijk besluit van 07 mei 2024 dat de wijzigingen in de nomenclatuur en de terugbetaling weergeeft: Koninklijk Besluit van 07 mei 2024
NOMENCLATUUR
Meer informatie op de RIZIV website:
- Artsen: Introductie van de HPV-test als primaire screeningstest voor de opsporing van baarmoederhalskanker in België | RIZIV
- Laboratoria: Introductie van de HPV-test als primaire screeningstest voor de opsporing van baarmoederhalskanker in België | RIZIV
- Aanpassing van de nomenclatuur van Artikel 3
-
The nomenclatuur van Artikel 3 voor het nemen van een cervicovaginaal uitstrijkpreparaat is aangepast. Aan de bestaande nomenclatuur (voor screening en diagnostische/therapeutische opvolging) werd een derde verstrekking toegevoegd voor klinisch/diagnostisch onderzoek (verdachte symptomatologie), waar ook screening bij hoog-risicogroepen onder valt — enkel terugbetaald na notificatie: Notificatie Formulier
U vindt de nomenclatuur met de toepassingsregels (frequentie van aanrekenen en leeftijdscategorie) in NomenSoft — RIZIV
NOMENCLATURE CODES: SMEAR COLLECTION
General practitioner
Gynaecologist
1
Screening
114030-114041
114170-114181
2
Opvolging: diagnostisch/therapeutisch
149612-149623
149634-149645
3
NIEUW: klinisch/diagnostisch + hoog-risicogroepen
114192-114203
149656-149660
- Aanpassing van de nomenclatuur van Artikel 14, g)
-
De nomenclatuur van Artikel 14, g) is ook aangepast (431955-431966): het honorarium voor de colposcopie werd aanzienlijk verhoogd.
Tegelijkertijd werden er kwaliteitseisen gesteld met:
- een verplichte deelname aan een gevalideerde colposcopiecursus of het behalen van een colposcopiecertificaat voor de uitvoerende gynaecoloog, georganiseerd door VVOG/CRGOLFB;
- een verplichte opslag van interpreteerbare beelden in het medisch dossier van de patiënt;
- een verplicht gestandaardiseerd verslag met de minimale EFC-eisen (European Federation of Colposcopy) voor de beschrijving van de colposcopie.
De kwaliteitsrichtlijnen colposcopie :
 wetenschappelijke richtlijn hoofdstuk 6.
wetenschappelijke richtlijn hoofdstuk 6. - Overdracht van de nomenclatuur van Artikel 32 naar Artikel 24bis
-
De nomenclatuur voor HPV-testen is overgedragen van artikel 32 naar artikel 24bis. De nomenclatuur van artikel 24bis is toegankelijk voor zowel pathologen als klinisch biologen.
De aangepaste nomenclatuur van artikel 32 (alleen toegankelijk voor pathologen) voorziet in 4 aparte codes voor de cytologie :
NOMENCLATUURCODES: CYTOLOGIE
1
Primaire screening door cytologie bij 25- tot 29-jarigen en éénmalig bij verzekerden vanaf 65 jaar*
589853-589864
2
Reflexcytologie na een positieve HPV-test bij 30- tot 64-jarigen
591791-591802
3
Diagnostische of therapeutische opvolging: éénmaal per jaar (tenzij notificatie en tijdelijk hoog risico)
591813-591824
4
Bij klinische symptomen en testen van hoogrisicogroepen (via notificatie)
591835-591846
De nomenclatuur van Artikel 24bis voorziet in 4 aparte codes voor HPV-testen :
NOMENCLATURE CODES: HPV-test
1
Primaire HPV-screening bij 30- tot 64-jarigen en éénmalig bij verzekerden vanaf 65 jaar*
553615-553626
2
Reflex HPV-test bij afwijkende cytologie bij 25- tot 29-jarigen
553630-553641
3
Diagnostische of therapeutische opvolging: éénmaal per jaar (tenzij notificatie en tijdelijk hoog risico)
553652-553663
4
Bij klinische symptomen en testen van hoogrisicogroepen (via notificatie)
553674-553685
- *Indien de afgelopen 10 jaar geen screening werd terugbetaald
REMGELD & SUPPLEMENTEN
- Remgeld en supplementen
-
In het kader van de primaire screening wordt ernaar gestreefd het remgeld te beperken om de drempel tot deelname zo laag mogelijk te houden. De verzekerde betaalt geen persoonlijk aandeel voor:
- de afname van het uitstrijkpreparaat,
- de primaire screeningstest,
- de reflextesten — uitgevoerd na een positieve primaire screening
Er is wel remgeld verschuldigd voor de raadpleging bij de gynaecoloog of de huisarts.
Het Koninklijk Besluit van 30 Oktober 2017 (BS 30/10/2017, numac 2017013750) bepaalt dat er geen supplementen mogen worden aangerekend voor geneeskundige verstrekkingen in het kader van georganiseerde screeningprogramma’s. Geen supplementen dus voor primaire screening en reflextesten.
Het Koninklijk Besluit: NL / FR
3. Bijzondere bepalingen voor de accreditatie van medische laboratoria
In samenwerking met Belgische Accreditatie-Instelling (Belac)
- Kwaliteit van de HPV testen en analyses (BELAC)
-
Om de kwaliteit van de HPV-testen en de analyses te waarborgen, moeten de HPV-testen uitgevoerd worden in een laboratorium dat door de minister van Volksgezondheid is erkend als laboratorium voor klinische biologie of pathologische anatomie. Het laboratorium moet ook een ISO 15189-accreditatie bezitten voor de uitgevoerde moleculaire testen uit art. 24bis. Het laboratorium moet bovendien de kwaliteitscontroles van Sciensano ondergaan. Bovendien moeten laboratoria specifiek worden geaccrediteerd voor een gevalideerde test uit de lijst van het NRC-HPV.
Bezoek de pagina van het National Reference Center (NRC) for Human papillomavirus
Voor cytologie kan een BELAC-accreditatie volgens ISO 15189 wettelijk niet verplicht worden opgelegd. De kwaliteit van de gynaecologische cytologie wordt eveneens gecontroleerd door Sciensano.
BELAC zal een richtlijn publiceren in de documentenreeks 2-405 waardoor de bepalingen van de richtlijn bindend worden voor de laboratoria die een ISO 15189-accreditatie aanvragen voor de respectievelijke prestaties binnen de baarmoederhalskanker screening en triage die binnen het toepassingsgebied van de norm ISO 15189 vallen.
4. Lijst van geaccepteerde HPV-testen
In samenwerking met het Nationaal Referentiecentrum voor Human Papillomavirus (NRC-HPV)
- Internationaal gevalideerde hoog-risico HPV-testen
-
De lijst van internationaal gevalideerde hoog-risico HPV-testen die in België kunnen worden gebruikt voor screening op baarmoederhalskanker staat op:
Nationaal Referentiecentrum (NRC) voor Humaan papillomavirus | sciensano.be.
De tabel bevat een dynamische lijst van moleculaire testen voor de opsporing van hoog-risico HPV en zal minstens tweemaal per jaar bijgewerkt worden naarmate nieuw wetenschappelijk bewijs beschikbaar wordt.
5. Registratie van screeningresultaten
In samenwerking met Stichting Kankerregister (BCR)
- Belgian Cancer Registry
-
Zowel de laboratoria voor pathologische anatomie als de laboratoria voor klinische biologie hebben de wettelijke verplichting om gegevens over hun resultaten met betrekking tot de vroegopsporing van kanker te registreren bij de Stichting Kankerregister (Belgian Cancer Registry, BCR). Er bestaat daardoor een wettelijke basis voor BCR om gegevens over stalen van de baarmoederhals te verzamelen en op te nemen in het cyto-histo-pathologieregister. Bovendien moeten screeningsresultaten verplicht geregistreerd worden, overeenkomstig artikel 5a) van artikel 24bis van de nomenclatuur.
De praktische uitwerking hiervan werd maximaal afgestemd op reeds bestaande of toekomstige gegevensuitwisseling, in consensus met de respectievelijke beroepsorganisaties. Na validatie zal deze informatie beschikbaar zijn op laboratoria | Belgian Cancer Registry. Deze registratie is vereist voor alle resultaten van cervicale stalen, niet alleen voor deze van screeningsstalenLaboratoria voor klinische biologie naar BCR
Het BCR ontvangt een kopie van alle gevalideerde resultaten wanneer deze naar de aanvragende arts worden verzonden (= continue aanlevering). Daartoe worden individuele resultaten verzonden als gestructureerde berichten die voldoen aan de HL7-FHIR-standaard.
Laboratoria for Pathologische Anatomie naar BCR
De laboratoria leveren maandelijks twee aparte bestanden aan het BCR: een gestructureerd bestand met alle variabelen en een bestand met de schriftelijke rapporten (protocollen). Het BCR gaat een minimale uitbreiding implementeren van de huidige Cervibase-codes, om te kunnen rapporteren in de laesiecodes van CODAP/SNOMED wanneer alleen een HPV-test is uitgevoerd (zonder cytologie). In de toekomst zal ook deze registratie evolueren naar een continue aanlevering van individuele resultaten via gestructureerde berichten die voldoen aan de HL7-FHIR-standaard.1Art. 138, §2, 3°, a) Gecoördineerde Wet van 10 mei 2015 op de uitoefening van de gezondheidszorgberoepen, B.S. 18 juni 2015.
Voor de laboratoria voor pathologische anatomie is deze registratieverplichting ook opgenomen in de erkenningsregels: art. 35, 6° Koninklijk Besluit van 5 december 2011 betreffende de erkenning van de laboratoria voor pathologische anatomie door de Minister tot wiens bevoegdheid de Volksgezondheid behoort, B.S. 13 februari 2012.
6. Belangrijke implicaties voor laboratoria
In samenwerking met de Commissies en beroepsverenigingen Klinische Biologie / Pathologische Anatomie
- Klinische biologie
-
Enkele belangrijke implicaties voor de dagelijkse praktijk:
1. Er dient een geïntegreerd advies te worden geformuleerd door het laboratorium dat de primaire HPV test heeft uitgevoerd.
Het resultaat van de reflex cytologie wordt overgemaakt aan de zorgverlener die de primaire HPV test heeft uitgevoerd. Op basis van de resultaten van de primaire HPV test en het aanvullend cytologisch onderzoek zal het laboratorium dat de primaire HPV test heeft uitgevoerd een aanbeveling vetrekken betreffende de verder te volgen therapeutische houding.
- Geïntegreerd advies -25-29 en 30-64 -jarigen in de algemene bevolking

- ≥ ASC-H/AGC = ASC-H of een meer hooggradige afwijking (HSIL, SCC, AIS, AC) of AGC
INSU: ontoereikende cytologie, niet-representatief staal (gebrek aan epitheelcellen/onvoldoende celmateriaal, cellyse, overvloedig bloed, enz.)
HPVi: ontoereikend (inconclusief) HPV-testresultaat
NB: Met onmiddellijke doorverwijzing voor colposcopie wordt bedoeld binnen 3 maanden of sneller, afhankelijk van de ernst van het positieve screeningsresultaat.
Opgelet: Als bij cytologisch onderzoek normale endometriumcellen worden gevonden bij een rechthebbende > 45 jaar, wordt aanvullend advies gegeven: ‘Klinische correlatie is aangewezen om endometriumpathologie uit te sluiten bij postmenopauzale vrouwen’.
Opgelet: Als bij cytologisch onderzoek afwijkende endometriumcellen worden gevonden bij een rechthebbende (gelijk welke leeftijd), wordt aanvullend advies gegeven: ‘Exploratie om endometriumpathologie uit te sluiten’.
Vetgedrukt: het daadwerkelijke geïntegreerde advies, nadat stalen verzonden waren om reflextesten uit te voeren.
Meer informatie in
 wetenschappelijke richtlijn hoofdstuk 2.4.
wetenschappelijke richtlijn hoofdstuk 2.4. ANNEX 1
ANNEX 1
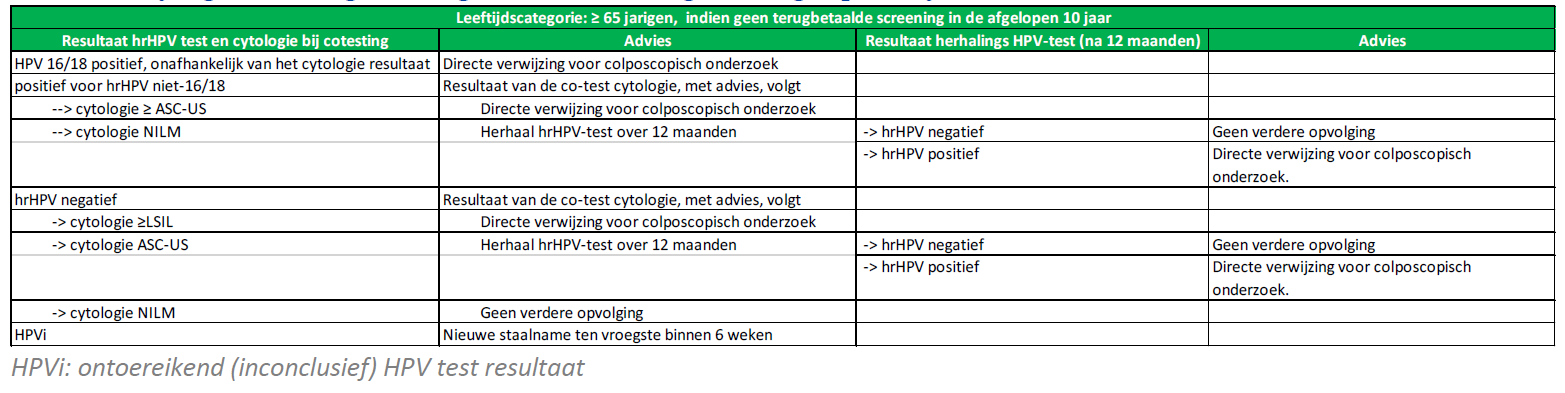
- advies: ≥65 -jarigen, indien geen terugbetaalde screening in de afgelopen 10 jaar
Meer informatie in
 wetenschappelijke richtlijn hoofdstuk 2.5.
wetenschappelijke richtlijn hoofdstuk 2.5. ANNEX 2
ANNEX 22. Een snelle rapportage naar het Belgisch kankerregister is nodig (Cfr. Registratie van screeningresultaten).
- Geïntegreerd advies -25-29 en 30-64 -jarigen in de algemene bevolking
- Pathologische anatomie
-
Voor de laboratoria pathologische anatomie is er geen onmiddellijke verandering in de manier waarop de data worden geëxtraheerd en aangeleverd aan het kankerregister. Echter de frequentie wordt opgedreven van 1x per kwartaal naar 1x per maand. Er wordt ook een uitbreiding voorzien van de CODAP codes voor de codering van de HPV testen: HPV+, HPV- en HPVi worden toegevoegd aan de CODAP codes als onderdeel van de Cervibase codes.
In de toekomst zal ook deze registratie evolueren naar een continue aanlevering van individuele resultaten via gestructureerde berichten die voldoen aan de HL7-FHIR-standaard (Cfr. Registratie van screeningresultaten).
Een geïntegreerd advies dient te worden geformuleerd door het laboratorium dat de primaire screeningstest heeft uitgevoerd.
Het resultaat van de reflex test wordt overgemaakt aan de zorgverlener die de primaire screeningstest heeft uitgevoerd. Op basis van de resultaten van zowel de primaire screeningstest en de aanvullende reflex test zal het laboratorium dat de primaire screeningstest heeft uitgevoerd een aanbeveling vetrekken betreffende de verder te volgen therapeutische houding.
Geïntegreerd advies voor -25-29 en 30-64 -jarigen in de algemene bevolking
≥ ASC-H/AGC = ASC-H of een meer hooggradige afwijking (HSIL, SCC, AIS, AC) of AGC
INSU: ontoereikende cytologie, niet-representatief staal (gebrek aan epitheelcellen/onvoldoende celmateriaal, cellyse, overvloedig bloed, enz.)
HPVi: ontoereikend (inconclusief) HPV-testresultaat
NB: Met onmiddellijke doorverwijzing voor colposcopie wordt bedoeld binnen 3 maanden of sneller, afhankelijk van de ernst van het positieve screeningsresultaat.
Opgelet: Als bij cytologisch onderzoek normale endometriumcellen worden gevonden bij een rechthebbende > 45 jaar, wordt aanvullend advies gegeven: ‘Klinische correlatie is aangewezen om endometriumpathologie uit te sluiten bij postmenopauzale vrouwen’.
Opgelet: Als bij cytologisch onderzoek afwijkende endometriumcellen worden gevonden bij een rechthebbende (gelijk welke leeftijd), wordt aanvullend advies gegeven: ‘Exploratie om endometriumpathologie uit te sluiten’.
Vetgedrukt: het daadwerkelijke geïntegreerde advies, nadat stalen verzonden waren om reflextesten uit te voeren.More information in
 wetenschappelijke richtlijn hoofdstuk 2.4
wetenschappelijke richtlijn hoofdstuk 2.4 ANNEX 1
ANNEX 1
Geïntegreerd advies ≥65 -jarigen, indien geen terugbetaalde screening in de afgelopen 10 jaar

Meer informatie in
 wetenschappelijke richtlijn hoofdstuk 2.5.
wetenschappelijke richtlijn hoofdstuk 2.5. ANNEX 2
ANNEX 2
7. Regio-specifieke details in verband met het bevolkingsonderzoek
- Organisaties die het bevolkingsonderzoek organiseren
-
Vlaanderen*
Departement Zorg & CvKO
Brussels
Vivalis & BruPrev
Wallonië
AVIQ & CCRef
Duitstalige gemeenschap
CCRef
* Het Centrum voor Kankerscreening (CvKO) stuurt een uitnodigingsbrief naar alle vrouwen in de doelgroep (25-64j) en stuurt ook het screeningsresultaat, datum laatste screening, datum volgende uitnodiging en (geïntegreerd) advies door naar de GMD-arts van de vrouw (arts die het Globaal Medisch Dossier beheert) en mijngezondheid.be; te raadplegen door de vrouw en/of andere behandelende artsen.
Lees het volledige document van de wetenschappelijke richtlijn
Terug naar baarmoederhalskankerscreening


